胞内酸碱度(pH)是重要的生化信号,与细胞生理功能紧密相关,但细胞如何感知及适应胞内pH变化仍然未知。同济大学医学院/附属东方医院章小清/刘玲/房玉江团队前期研究创新性地发现了Smad5是细胞内的共性酸碱度感受器,实时感知胞外微环境,包括温度、酸碱度和渗透压改变所导致的胞内pH变化,进而通过调控代谢反应来维持胞内能量稳态。研究团队提出细胞中存在一条共性的胞内pH-Smad5信号转导通路的初步构想。
3月20日,章小清/刘玲/房玉江团队在国际顶级学术期刊《细胞·代谢》(Cell Metabolism)上发表了题为“Cytosolic pH is a direct nexus in linking environmental cues with insulin processing and secretion in pancreatic β cells”的研究成果。研究发现胞内pH-Smad5信号通路调控胰岛素加工与分泌的全新生理功能,该通路异常是糖尿病发生发展的重要病理生理机制,为糖尿病的干预提供了新的视角。

研究人员通过建立酸碱报告模型小鼠,发现高糖刺激会引起胰腺β细胞GFP-Smad5从细胞核转位至细胞浆,说明高糖刺激引起β细胞胞内pH升高。为了探究这一现象的生理病理意义,研究人员在胰腺β细胞条件敲除Smad5,敲除Smad5引起小鼠高血糖及糖耐量异常,并进一步证实敲除Smad5引起小鼠高血糖的原因是胰岛素分泌水平降低及胰岛素原表达增加,说明敲除Smad5引起胰岛素加工过程受阻。机制方面,研究人员证明Smad5与V-ATPase(胰岛素分泌囊泡酸化的关键调节酶)的亚基ATP6V1A结合,促进V-ATPase酶活性,并加速分泌囊泡酸化,从而促进由胰岛素原剪切为成熟胰岛素的加工过程。
为了解析胞内pH-Smad5信号通路在糖尿病发生发展中的作用,研究人员发现高脂饮食诱导的2型糖尿病模型小鼠,β细胞GFP-Smad5向细胞核内聚集,说明β细胞胞内酸化,并进一步证实这一酸化抑制胞内pH-Smad5信号,削弱胰岛素加工过程。而通过模拟β细胞胞内碱化的Smad5突变体小鼠或长期小苏打碱性饮水可以矫正β细胞胞内酸化,促进胰岛素加工并有效减轻高脂饮食诱导的糖耐量异常表型。
该研究首次在体内证实了胞内pH-Smad5信号通路的生理病理功能,揭示了这一通路异常在糖尿病发病中的病理生理机制,以及通过模拟胞浆碱化来改善糖尿病胰岛素分泌不足表型,为糖尿病的防治提供了新的思路。
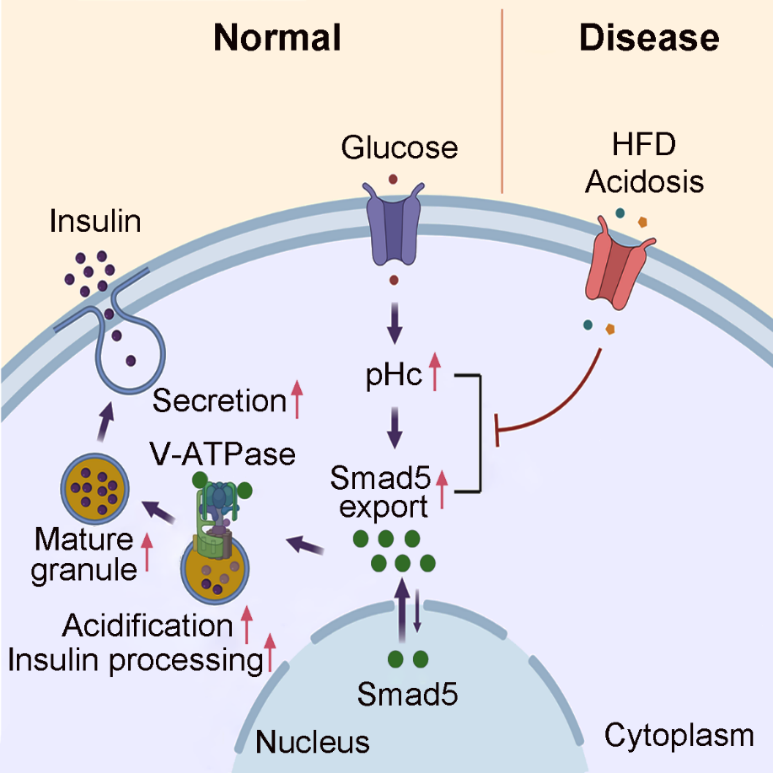
胞内pH-Smad5通路调控胰岛素加工与分泌机制
章小清/刘玲/房玉江研究团队经过十余年专注研究探索,在领域内率先发现了胞内pH感受器,初步建立了胞内pH-Smad5信号转导通路的概念,并在体内体外研究了这一通路的生理病理意义。研究团队通过解析胞内pH的共性感受器,为研究胞内pH这一重要信号提供了前所未有的手段,同时将胞内pH存在重要生物学功能这一设想通过体内体外模型进行了证实,有望快速推进相关领域研究。
同济大学医学院/附属东方医院章小清教授、刘玲教授、房玉江助理教授为论文共同通讯作者,同济大学医学院房玉江助理教授、冯和玺博士、张博文博士为共同第一作者。该研究工作得到国家自然科学基金委、科技部、上海市的资助。
论文链接:https://doi.org/10.1016/j.cmet.2024.02.012
